1. 研究課題
 本部門では、発生や再生、進化の仕組みを、ゲノム・エピゲノム制御の側面から解明することを目的として、下記の研究課題1)〜3)に取り組んでいます。研究材料には、主に2種類のツメガエル(アフリカツメガエルとネッタイツメガエル)とリュウキュウカジカガエルを用いています。部門長はネッタイツメガエルを用いた実験系の開発者であり、高効率なトランスジェネシス技術の開発や(I-SceI法、Nature Protocol 1: 1703-1710 (2006)、Dev. Growth Differ. 51: 387-401 (2009))、全ゲノム配列の解読(毎日新聞、日本経済新聞他で報道、Science 328: 633-636 (2010))等に携わってきました。実験には、これらのトランスジェネシス技術やゲノム編集技術、蛍光タンパク質を用いた生体イメージング、次世代シーケンサーを用いたトランスクリプトーム解析、クロマチン免疫沈降、比較ゲノム解析等、ウェットからドライまで様々な先鋭的方法を駆使しています。
本部門では、発生や再生、進化の仕組みを、ゲノム・エピゲノム制御の側面から解明することを目的として、下記の研究課題1)〜3)に取り組んでいます。研究材料には、主に2種類のツメガエル(アフリカツメガエルとネッタイツメガエル)とリュウキュウカジカガエルを用いています。部門長はネッタイツメガエルを用いた実験系の開発者であり、高効率なトランスジェネシス技術の開発や(I-SceI法、Nature Protocol 1: 1703-1710 (2006)、Dev. Growth Differ. 51: 387-401 (2009))、全ゲノム配列の解読(毎日新聞、日本経済新聞他で報道、Science 328: 633-636 (2010))等に携わってきました。実験には、これらのトランスジェネシス技術やゲノム編集技術、蛍光タンパク質を用いた生体イメージング、次世代シーケンサーを用いたトランスクリプトーム解析、クロマチン免疫沈降、比較ゲノム解析等、ウェットからドライまで様々な先鋭的方法を駆使しています。
1) ゲノム重複に伴う遺伝子進化の研究
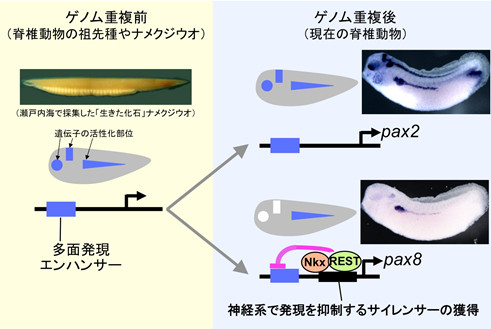 これまでの研究から、5億年以上前のカンブリア紀に、脊椎動物の祖先種において、全ての遺伝子のコピー数が倍に増える「全ゲノム重複」とよばれる現象が起きたことがわかっています。これにより余剰な遺伝子が生まれ、その発現パターンが多様化した結果、より複雑な体が進化したと考えられています。しかし具体的には、遺伝子の発現調節配列(シス調節配列)のどのような変化によって、この発現パターンの変化が引き起こされたのか、不明なままでした。この問題に対して私達は、眼や脳、腎臓の形成を制御するPax遺伝子ファミリーに注目し、その発現調節の仕組みをツメガエル、マウス、そして脊椎動物の祖先種に近縁で「生きた化石」とよばれるナメクジウオとの間で、トランスジェニック実験により比較解析しました。その結果、遺伝子の発現調節配列のうち活性化に働く部分(エンハンサー)は、重複遺伝子の間であまり変化していませんでしたが、このエンハンサーの作用を部分的に打ち消す配列(サイレンサー)が、重複遺伝子の片方に新たに付加され、発現パターンが大きく変化したことを発見しました。これは、遺伝子発現のおおまかな下絵が、エンハンサーよって5億年以上も昔の祖先種で既に完成していたこと、そして全ゲノム重複により遺伝子のコピー数が増えた後に、増えた遺伝子が必要な場所だけで働き、余計な場所では働かないように、サイレンサーが付け加わっていったことを示唆しています(毎日新聞、産經新聞他で報道、Nature Communications 3: 848 (2012))。
これまでの研究から、5億年以上前のカンブリア紀に、脊椎動物の祖先種において、全ての遺伝子のコピー数が倍に増える「全ゲノム重複」とよばれる現象が起きたことがわかっています。これにより余剰な遺伝子が生まれ、その発現パターンが多様化した結果、より複雑な体が進化したと考えられています。しかし具体的には、遺伝子の発現調節配列(シス調節配列)のどのような変化によって、この発現パターンの変化が引き起こされたのか、不明なままでした。この問題に対して私達は、眼や脳、腎臓の形成を制御するPax遺伝子ファミリーに注目し、その発現調節の仕組みをツメガエル、マウス、そして脊椎動物の祖先種に近縁で「生きた化石」とよばれるナメクジウオとの間で、トランスジェニック実験により比較解析しました。その結果、遺伝子の発現調節配列のうち活性化に働く部分(エンハンサー)は、重複遺伝子の間であまり変化していませんでしたが、このエンハンサーの作用を部分的に打ち消す配列(サイレンサー)が、重複遺伝子の片方に新たに付加され、発現パターンが大きく変化したことを発見しました。これは、遺伝子発現のおおまかな下絵が、エンハンサーよって5億年以上も昔の祖先種で既に完成していたこと、そして全ゲノム重複により遺伝子のコピー数が増えた後に、増えた遺伝子が必要な場所だけで働き、余計な場所では働かないように、サイレンサーが付け加わっていったことを示唆しています(毎日新聞、産經新聞他で報道、Nature Communications 3: 848 (2012))。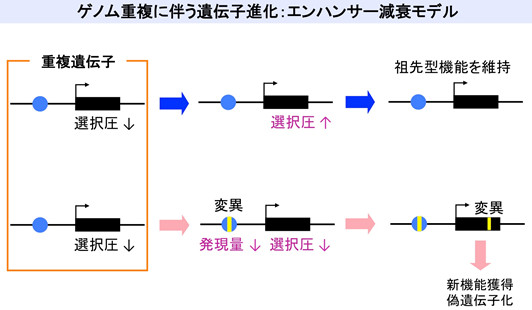 また、脊椎動物のグループにおいて、ゲノム重複はその祖先種のみならず、その後も様々な種の分岐過程で起きたことが知られています。両生類では、ネッタイツメガエルとアフリカツメガエルの祖先種が分岐した後、わずか1700万年ほど前にアフリカツメガエルの系譜で全ゲノム重複が起きました。私達はゲノム重複後の遺伝子進化の始まりとはどのようなものかを解明する為、Six6とよばれる眼形成遺伝子に注目し、ネッタイツメガエルが1つだけもつ祖先型と、アフリカツメガエルで2つに増えたコピーについて比較研究をおこないました。その結果、アフリカツメガエルの2つのSix6遺伝子のうち、1つのコピーのエンハンサーに変異が蓄積して発現量が低下し、それに伴って同じコピーのコード配列にもアミノ酸置換を伴う変異が蓄積していることを発見しました。このことは、同じ機能をもつ遺伝子が2つできた後に、一旦片方のコピーの発現量が低下するとそのコピーに対する選択圧が低下し、コード配列にも変異が蓄積し易くなることを示唆しています(Dev. Biol., 427: 84-92 (2017))。また興味深いことに、アフリカツメガエルのSix6遺伝子の1つに見つかったアミノ酸置換変異と類似した変異が、ヒトの小眼症患者に見つかっています。現在は、進化における遺伝子変異と、疾患の原因となる遺伝子変異との相関関係について研究を進めています。
また、脊椎動物のグループにおいて、ゲノム重複はその祖先種のみならず、その後も様々な種の分岐過程で起きたことが知られています。両生類では、ネッタイツメガエルとアフリカツメガエルの祖先種が分岐した後、わずか1700万年ほど前にアフリカツメガエルの系譜で全ゲノム重複が起きました。私達はゲノム重複後の遺伝子進化の始まりとはどのようなものかを解明する為、Six6とよばれる眼形成遺伝子に注目し、ネッタイツメガエルが1つだけもつ祖先型と、アフリカツメガエルで2つに増えたコピーについて比較研究をおこないました。その結果、アフリカツメガエルの2つのSix6遺伝子のうち、1つのコピーのエンハンサーに変異が蓄積して発現量が低下し、それに伴って同じコピーのコード配列にもアミノ酸置換を伴う変異が蓄積していることを発見しました。このことは、同じ機能をもつ遺伝子が2つできた後に、一旦片方のコピーの発現量が低下するとそのコピーに対する選択圧が低下し、コード配列にも変異が蓄積し易くなることを示唆しています(Dev. Biol., 427: 84-92 (2017))。また興味深いことに、アフリカツメガエルのSix6遺伝子の1つに見つかったアミノ酸置換変異と類似した変異が、ヒトの小眼症患者に見つかっています。現在は、進化における遺伝子変異と、疾患の原因となる遺伝子変異との相関関係について研究を進めています。
2) 眼の発生進化におけるエピジェネティック制御の研究
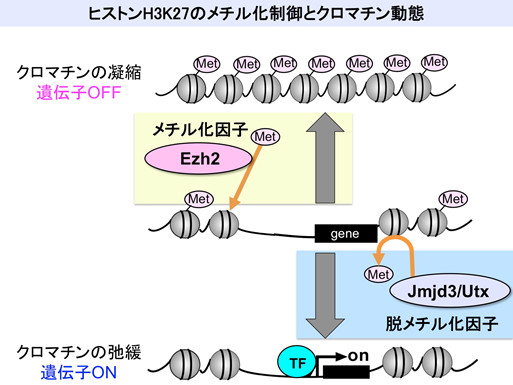 近年、遺伝子の発現調節におけるクロマチン構造制御の重要性が、様々な研究から明らかにされてきました。クロマチンの部位特異的な凝縮と弛緩は、その部位に含まれる遺伝子の転写抑制と活性化に働きますが、それらの制御にはヒストンのメチル化やアセチル化が重要な役割を果たします。また、これら遺伝子ごとのメチル化修飾やアセチル化修飾のパターンは、細胞分裂を経て娘細胞に引き継がれる為、いわば細胞記憶として働きます。私達はこれらのヒストン修飾の中でも、特にクロマチン凝縮に作用するヒストンH3K27メチル化因子群(ポリコームPRC2複合体構成因子群)と、それらに拮抗する脱メチル化因子群に注目して研究を進めています。その結果、発生においては、H3K27脱メチル化因子が感覚器プラコード(眼のレンズや鼻の嗅上皮、耳の内耳等の感覚器の共通原基)で発現し、この感覚器プラコードの一部からレンズが分化するのに必要なことを発見しました。これらの感覚器は、ナメクジウオのような原始的な脊索動物から脊椎動物が進化する過程で獲得された器官と考えられています。それゆえ、眼の進化におけるH3K27脱メチル化因子の役割についても研究を進めています。
近年、遺伝子の発現調節におけるクロマチン構造制御の重要性が、様々な研究から明らかにされてきました。クロマチンの部位特異的な凝縮と弛緩は、その部位に含まれる遺伝子の転写抑制と活性化に働きますが、それらの制御にはヒストンのメチル化やアセチル化が重要な役割を果たします。また、これら遺伝子ごとのメチル化修飾やアセチル化修飾のパターンは、細胞分裂を経て娘細胞に引き継がれる為、いわば細胞記憶として働きます。私達はこれらのヒストン修飾の中でも、特にクロマチン凝縮に作用するヒストンH3K27メチル化因子群(ポリコームPRC2複合体構成因子群)と、それらに拮抗する脱メチル化因子群に注目して研究を進めています。その結果、発生においては、H3K27脱メチル化因子が感覚器プラコード(眼のレンズや鼻の嗅上皮、耳の内耳等の感覚器の共通原基)で発現し、この感覚器プラコードの一部からレンズが分化するのに必要なことを発見しました。これらの感覚器は、ナメクジウオのような原始的な脊索動物から脊椎動物が進化する過程で獲得された器官と考えられています。それゆえ、眼の進化におけるH3K27脱メチル化因子の役割についても研究を進めています。
3) 脊髄再生におけるエピジェネティック制御の研究
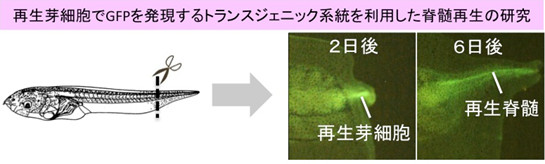 私達ヒトを含む哺乳類は、事故などで損傷した脊髄を十分に再生することができません。しかしツメガエル幼生は、脊髄を含む尾部を切断しても2週間ほどで再生することができます。この再生過程は様々な種類の幹細胞の増殖と分化を伴い、そこでは非常に多くの遺伝子の発現が抑制あるいは活性化されます。私達は、このゲノムワイドな遺伝子発現の切替えにH3K27メチル化因子群とそれらに拮抗脱メチル化群の両方が必要なことを発見しました。現在、それらのメチル化制御因子群の標的遺伝子の探索を進めています。
私達ヒトを含む哺乳類は、事故などで損傷した脊髄を十分に再生することができません。しかしツメガエル幼生は、脊髄を含む尾部を切断しても2週間ほどで再生することができます。この再生過程は様々な種類の幹細胞の増殖と分化を伴い、そこでは非常に多くの遺伝子の発現が抑制あるいは活性化されます。私達は、このゲノムワイドな遺伝子発現の切替えにH3K27メチル化因子群とそれらに拮抗脱メチル化群の両方が必要なことを発見しました。現在、それらのメチル化制御因子群の標的遺伝子の探索を進めています。
4) 生物の環境適応における遺伝子進化・ゲノム進化の研究
 現在地球上に存在するすべての生物は、それぞれの生息環境に適応することで生存し、多様な種生態を持つに至っています。そうした様々な生物の特徴はどのような遺伝子やゲノム構造の変化によってもたらされるのでしょうか。特に、温度への適応はすべての生物が避けられない環境要素です。また、我々ヒトをはじめとする恒温生物は温度を一定に保つことで分布を広げていますが、そもそもどのようにして37℃という高温に適応したのでしょうか。私達は、琉球列島に生息するリュウキュウカジカガエルが高温耐性を獲得し、幼生が40℃を越える温泉に生息していることを発見しました。これは両生類が生息する水温の世界最高記録です。私達はこのリュウキュウカジカガエルとその近縁種について、高温耐性関連遺伝子の単離と機能解析を行うとともに、全ゲノムシークエンス解読を進めています。
現在地球上に存在するすべての生物は、それぞれの生息環境に適応することで生存し、多様な種生態を持つに至っています。そうした様々な生物の特徴はどのような遺伝子やゲノム構造の変化によってもたらされるのでしょうか。特に、温度への適応はすべての生物が避けられない環境要素です。また、我々ヒトをはじめとする恒温生物は温度を一定に保つことで分布を広げていますが、そもそもどのようにして37℃という高温に適応したのでしょうか。私達は、琉球列島に生息するリュウキュウカジカガエルが高温耐性を獲得し、幼生が40℃を越える温泉に生息していることを発見しました。これは両生類が生息する水温の世界最高記録です。私達はこのリュウキュウカジカガエルとその近縁種について、高温耐性関連遺伝子の単離と機能解析を行うとともに、全ゲノムシークエンス解読を進めています。
5) 上皮性器官の形成機構とヒト先天異常に関する研究
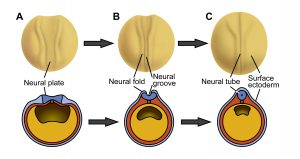
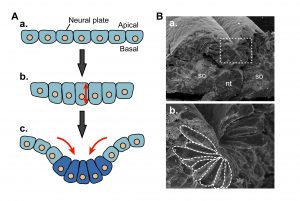
上皮性器官は上皮細胞の集団が管状や凹凸状の立体構造を取ることで形成される動物の基本的な生体構造です。なかでも、わたしたちの脳や脊髄のもとになる神経管は平面の細胞シートから管をつくることによって形づくられます(図1)。この神経管が形成される過程(神経管形成)では細胞の形態が細長く変化し(細胞伸長)、加えてくさび型へ変化する(頂端収縮)ことが重要です (図2、Dev. Growth Differ., 54, 266-276, 2012)。私達はツメガエルの神経管をモデルとした細胞生物学的な解析により、上皮性器官の形成に関わる細胞・細胞骨格の動態やその制御機構を明らかにしようとしています。
この研究は、神経管形成が正常に起こらないヒトの先天異常(神経管閉鎖障害)や様々な上皮形態形成異常を伴う疾患の原因解明にもつながる研究です。
2. バイオリソース事業
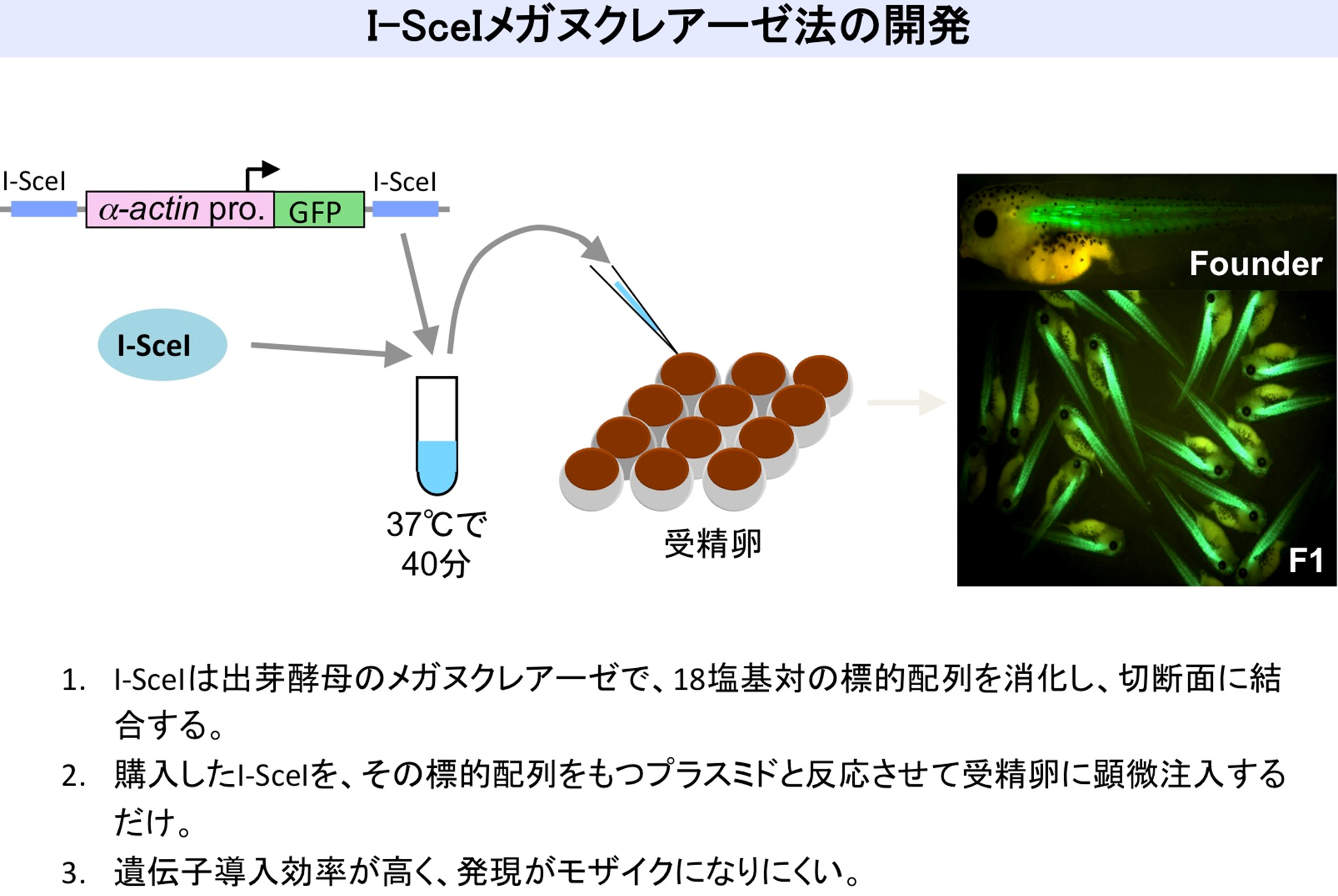
 現在、モデル両生類として分子生物学研究に汎用されているツメガエルには、アフリカツメガエル(Xenopus laevis)とネッタイツメガエル(Xenopus tropicalis)があります。アフリカツメガエルは古くから研究に用いられてきた種で、とても丈夫で飼育が容易なうえ、卵や胚が大きくマイクロインジェクションや組織移植等の実験を簡単におこなうことができます。トランスジェネシスについても、精子核移植法やI-SceIメガヌクレアーゼ法を用いれば、1日に200-300個体のファウンダーを容易に得ることができます。野生型近交系も、新潟大学の井筒ゆみ准教授らが作出したJ系統とよばれるものがあり、全ゲノム配列の解読に用いられました。しかしながら、世代時間が1年以上と長く、四倍体ゲノムをもつ為、遺伝学的研究には使いづらいという弱点もあります。
現在、モデル両生類として分子生物学研究に汎用されているツメガエルには、アフリカツメガエル(Xenopus laevis)とネッタイツメガエル(Xenopus tropicalis)があります。アフリカツメガエルは古くから研究に用いられてきた種で、とても丈夫で飼育が容易なうえ、卵や胚が大きくマイクロインジェクションや組織移植等の実験を簡単におこなうことができます。トランスジェネシスについても、精子核移植法やI-SceIメガヌクレアーゼ法を用いれば、1日に200-300個体のファウンダーを容易に得ることができます。野生型近交系も、新潟大学の井筒ゆみ准教授らが作出したJ系統とよばれるものがあり、全ゲノム配列の解読に用いられました。しかしながら、世代時間が1年以上と長く、四倍体ゲノムをもつ為、遺伝学的研究には使いづらいという弱点もあります。
一方、ネッタイツメガエルは世代時間が4−6ヶ月と短く、2倍体の小さなゲノムをもつ為、遺伝学的研究に適しています。トランスジェネシスについては、I-SceIメガヌクレアーゼ法により、1日に200-300個体のファウンダーを容易に得ることができます。全ゲノム配列も解読されており、遺伝子破壊はCRISPR/Cas9法等により簡単におこなうことができます。しかし、飼育にはアフリカツメガエルより厳しい水質管理が必要です。また卵や胚が小さい為(体積でアフリカツメガエルの1/3ぐらい)、マイクロインジェクション等の実験には多少の慣れが必要です。
ポストゲノム時代を迎えた現在、ツメガエルを用いた発生や再生、進化の研究には、ゲノム編集による遺伝子破壊と、その結果解析の方法として、生体イメージング解析やトランスクリプトーム解析等を有効に用いることが必要です。これらツメガエル以外にも、アホロートルはモデル両生類として汎用されています。また次世代シーケンサー解析が普及した今、様々な在来種のカエルやイモリが新しい実験動物や遺伝子資源として重要になりつつあります。私達の研究室では、研究コミュニティの支援を目的として、これらの両生類を扱う以下のバイオリソース事業を実施しています。
1) ネッタイツメガエル・ナショナルバイオリソースプロジェクト(NBRP)
AMED(日本医療研究開発機構)の支援事業として、主に4種類のネッタイツメガエル野生型近交系(Nigerian A, Nigerian H, Golden, Ivory Coast)の改良・維持・配布、及びそれらを用いて作製された組換え体の収集・維持・配布をおこなっています。Nigerian Aは、全ゲノム配列解読に用いられた個体の直系系統です。Nigerian HはNigerian Aに近い派生系統で、Nigerian Aより産卵数が多い傾向があります。GoldenはNigerian Aに対してNigerian Hより遺伝的に離れていますが、飼育が容易で使い易い系統です。Ivory CoastはNigerian Aから最も遺伝的に離れていますが、受精率が安定して高く使い易い系統です。組換え体としては、特定の組織や器官、例えば脳神経系や血管系をGFPタンパク質で標識したような生体イメージング解析用のトランスジェニック系統や、ゲノム編集によって作製された汎用性のある変異体(疾患モデル等)の収集・維持・配布を進めています。詳しくは本センターHPのトップに掲載されたリンクより、ネッタイツメガエルNBRPのウェブサイトをご覧下さい。
2) その他のモデル両生類や在来種のリソース事業(系統維持班)
 アフリカツメガエルについては、野生型近交系(J系統)や、シグナル伝達系の阻害因子を発現するトランスジェニック系統、生体イメージング解析用に特定の組織でGFPを発現するトランスジェニック系統等の開発・収集・維持・配布をおこなっています。アホロートルに関しては、野生型やアルビノの近交系の収集・維持・配布をおこなっています(現在、提供可能な系統のリストを準備中です。)。
アフリカツメガエルについては、野生型近交系(J系統)や、シグナル伝達系の阻害因子を発現するトランスジェニック系統、生体イメージング解析用に特定の組織でGFPを発現するトランスジェニック系統等の開発・収集・維持・配布をおこなっています。アホロートルに関しては、野生型やアルビノの近交系の収集・維持・配布をおこなっています(現在、提供可能な系統のリストを準備中です。)。
3. OB・OGの進路
(部門長が前任校で主宰していた研究グループのOB・OGを含みます。)
大学教員2名(准教授1名、助教1名)
博士研究員1名(現在オーストリアの著名研究室で活躍中)
その他、他大学大学院生(京都大学大学院医学研究科、奈良先端科学技術大学院大学、長浜バイオ大学等)、製薬会社研究職、食品会社研究職、種苗会社、食品会社、工場衛生管理会社、食品系貿易会社、公務員、農協等。